Configuración electrónica del Renio
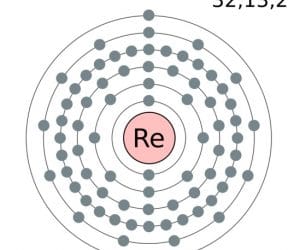
Fue descubierto en el año 1925 por tres científicos de origen alemán. Este elemento no se encuentra en la naturaleza en estado elemental y hasta la fecha no ha sido hallado alguna mena mineral. La molibdenita y la gadolinita son las menas de donde se puede extraer un poco el renio. Al igual que el tecnecio, se oxida en temperaturas muy altas de oxígeno.
Sus estados de oxidación son 2, 3, 4, 6, 7, su configuración electrónica es Xe 4f145d56s2 y configuración simplificada es 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 4f14 5d5 6s2.
Configuración electrónica simplificada del renio

De acuerdo con su configuración electrónica, estos están repartidos de la siguiente manera: 5s2 5p6 4f14 5d5 6s2
- 2 electrones en la órbita 1s
- 2 electrones en la órbita 2s
- 6 electrones en la órbita 2p
- 2 electrones en la órbita 3s
- 6 electrones en la órbita 3p
- 10 electrones en la órbita 3d
- 2 electrones en la órbita 4s
- 10 electrones en la órbita 4d
- 2 electrones en la órbita 5s
- 6 electrones en la órbita 5p
- 14 electrones en la órbita 4f
- 5 electrones en la órbita 5d
- 2 electrones en la órbita 6s
Características del renio
Tiene color plateado, por lo regular se produce como un polvo de color gris. Se hace posible la fabricación de objetos con este metal en estado puro al someterlo bajo presión al vacío y con calentándolo en presencia del hidrógeno. Sin embargo, la demanda que existe de estos objetos es muy mínima.
Isotopos del renio
En su forma natural el renio es 37.4 por ciento 185 Re, el cual es estable, y el 62,6 por ciento que, a pesar de ser inestable, cuenta con una vida útil media de 41,2 días por 109 años, lo que se considera muy larga. Además, existen varios isótopos de este elemento, de los que son los más longevos el 184m Re que tiene una vida de 169 días y el186 Re, cuya vida es de 200 mil años
También se conocen otros 33 isótopos inestables, de los cuales los de mayor tiempo de duración son el 183 que tiene una vida media de 70 días, el los más longevos son el 182Re que dura 64 horas, el 183Re con una vida media de 70 días, 184Re cuya vida es de 38 días, el 186 Re que dura 3,7186 días, y también el 189Re cuya vida es de 24,3 horas. La duración de vida del resto es menor a un día.
Producción del renio
Años antes de ser descubierto, hubo un poco de producción de molibdeno y en los años 50 fue cuando inició a ser rentable su comercialización, en momentos en que la utilización del renio en catalizadores establecer una demanda que se podía notar. A nivel global, la producción se encuentra anualmente en unas 5 toneladas y las reservas de este elemento rondan las 350 toneladas, hallándose sobre todo en menos estadounidenses, chilenas y rusas.
Usos del renio
- Debido a que es muy resistente, principalmente a la corrosión, es utilizado como material de contacto. Con este elemento además es fabricado un tupo de alambre especial usado en las cámaras fotográficas para el flash. También muy bueno en las aleaciones y como un aditivo metálico es de mucha utilidad.
- De manera ocasional ha sido usado para platear algunas joyas. También se utiliza como aditivo junto al molibdeno y el wolframio para la formación de aleaciones que se emplean en filamentos de lámparas y hornos.
- En la industria química se utiliza como catalizador, de manera particular en aquellos procesos que tienen relación con la adición de hidrógeno gas a otras moléculas.
Efectos del Renio en la salud y el medio ambiente
Sus propiedades toxicológicas todavía no se han investigado a totalidad, pero se sabe que puede irritar y causar quemaduras en los ojos y la piel, irritación del tracto respiratorio. En cuanto al ambiente, hasta el momento aún no hay registro de toxicidad.

Vea también...