Configuración electrónica del Actinio
Compone a las tierras raras y otorga el nombre a la serie de los actínidos. Es un metal radiactivo característicamente blando que brilla en la oscuridad. Los isótopos que tienen número másico entre el 219 y el 234 son los que se conocen de este elemento.
El de isótopo de mayor estabilidad es el Ac227 cuya vida media es de 21,7 años, este isótopo es hallado en el uranio natural bajo la proporción del 0,175% mientras que el Ac228 se halla en la naturaleza. Existen 22 isótopos artificiales de este elemento, cada uno de ellos es radiactivo y sus vidas medias son sumamente cortas. El actinio se descubrió en 1899, su uso principal es ser fuente de partículas alfa.
Elemento químico representado con el símbolo y número atómico Ac 89, forma parte del grupo 3 de los elementos de la tabla periódica. Se le considera como un actínido y es uno de los elementos de las tierras raras.
Fue descubierto por el químico André Louis Debierne en el año 1899 cuando trabajada con la pechblenda, quien lo caracterizó como una sustancia parecida al titanio, y en el 1900 como sustancia similar al torio. Posteriormente fue descubierto de forma independiente en el 1902 por Friedrich Oscar Giesel quien dio a conocer su parecido con el lantano nombrándolo en el 1904 como emanium. Se muestra como un metal con capacidad radioactiva y de textura blanda que se destaca con gran facilidad en la oscuridad.
Configuración Electrónica del Actinio
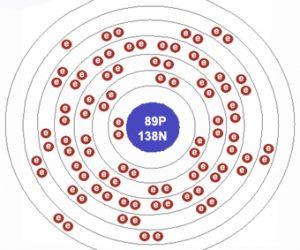
Con la configuración electrónica es posible especificar la manera en la que se estructuran los electrones ubicados en los átomos que un elemento tiene. El radio medio de este elemento es igual a 195 pm.
El actinio tiene 89 electrones en total, estos se distribuyen de la siguiente forma: la primera capa posee 2 electrones, en la segunda capa se encuentran 8, en la tercera capa se hallan 18 electrones, la cuarta capa tiene 32 electrones, en la quinta capa se encuentran 18, en la sexta hay 9 electrones, mientras que en la séptima y última se tiene sólo 2 electrones.
De acuerdo con la posición en la que se ubica el actinio en la tabla periódica de los elementos, el mismo está ubicado en el período 7 del grupo 3. La masa atómica de este elemento es de 2,7 u.
Propiedades del Actinio
El actinio se ubica en el grupo de los actínidos. Los actínidos poseen un número atómico mayor, no pueden ser localizados en la naturaleza y tienen un tiempo de vida relativamente corto. Cada uno de los isótopos pertenecientes al grupo de los actínidos, incluyendo al elemento actinio, se caracterizan por ser radiactivos.
El actinio es sólido en su forma natural. Este elemento químico tiene una tonalidad plateada, su símbolo químico es Ac y su número atómico es 89. Su punto de ebullición es de -269,15 grados centígrados o grados Celsius, que es igual a 3 grados Kelvin. El punto de fusión es de -271,15 grados centígrados o grados Celsius, similar a ser 1 grado Kelvin.
- Presenta una densidad de 10.070 kg/m3.
- Sus electores por capa: 2, 8, 18, 32, 18, 9,2.
- Su conductividad términa es de 12W (k.m).
- Se distingue por su apariencia plateada o metalizada.
- Su calor de fusión es de 62kJ/mol.
- Tiene una propiedad que supera a 150 veces la del radio, siendo ideal su uso en el análisis de trazas de minerales.
- Entre sus propiedades atómicas se destaca su radio atómico y el medio que es de 188 y 195 pm, su estado de oxidación de +3, su estructura cristalina que es cubica y su configuración electrónica representada por [Rn] 6d17s2.
- Las propiedades físicas que distinguen al Actinio es su punto de fusión y ebullición de 1051 y 3198 grados Celsius. Su estado ordinario que siempre se muestra en estado Sólido, su entalpía de fusión de 14,2(kJ.mol-1) y de vaporización de: 418 (kJ.mol-1). De igual forma se destaca su volumen molar / cm3mol-1 que es de 22.56, y su resistencia eléctrica que es de 20 grados Célsius.
- Es muy abundante en los océanos, en la atmósfera y en la corteza terrestre.
- Posee excelente propiedades térmicas.
- Es muy utilizado en investigaciones científicas, debido a su alta reactividad. Es perfecto en la producción de neutrones y en un futuro será un excelente tratamiento contra el cáncer.
- También se emplea para desarrollo de tecnología nuclear en la liberación de radioactividad a los suelos, atmósfera, mares, océanos y nivel acuífero.
Características Básicas del Actinio
- El actinio es metálico, tiene un color plateado, también es radiactivo similar a todos los demás actínidos. A causa de su enorme radiactividad, el elemento brilla en la oscuridad con una tonalidad azulada.
- El isótopo Ac227 es encontrado en los minerales de uranio pero solamente en trazas. Este emite partículas B y a que tienen un período de semidesintegración igual a 21,773 años. Una tonelada de mineral de uranio se compone de aproximadamente 0,1 g de actinio.
- El comportamiento químico de este elemento tiene mucha similitud con las demás tierras raras, principalmente con el lantano el cual es el elemento ubicado encima del mismo en la tabla periódica. El actinio también guarda similitudes con el radio, elemento localizado antes de el en la tabla. A pesar de esto, el actinio no posee electrones ubicados en el orbital 5f como sucede con los demás actínidos, sino que la configuración electrónica del elemento es 6d17s2. El radio iónico se relaciona al número de coordinación 4, por lo tanto es igual a 126.0 pm.
Otras características importantes de la configuración del actinio:
- Su nombre significa rayo o haz luminoso.
- Se produce como el isótopo del uranio 227Ac.
- Es altamente reactivo.
- Pertenece al período 7, grupo 3 y bloque F de la tabla periódica.
- Su nombre atómico es Actinio, su símbolo es Ac y el número atómico es el 89.
- Es muy parecido al resto de las tierras raras en cuanto a su comportamiento químico, en especial es similar al lantano y al radio, la diferencia de estos es que este elemento es carente en su orbital 5f de electrones.
- Elemento metálico y radiactivo de tono plateado.
- Tiene una intensa radiactividad que da una luz azulada en la oscuridad.
- Se encuentra como un producto intermedio en la serie radiactiva de desintegración y en cuanto al peso de la corteza representa el 5,5x10-14%.
- Su comportamiento es similar al resto de los elementos de las tierras raras, en especial al del lantano, el cual se ubica encima de él en la tabla periódica.
- Se puede extraer de ciertos elementos como es el AcBr3, AcF3, AcOCI, AcOF, AcPO4, Ac2O3 Y AcOBr.
Isótopos del Actinio
Los únicos isótopos que se hallan en la naturaleza son los radiactivos Ac227, tienen mayor estabilidad que los demás isótopos identificados. Su periodo de semidesintegracion es igual a 21,773 años. Después está el Ac225 que dura 10 días, el Ac226 tiene una duración de 29,37 horas y luego está el Ac228 con apenas 6,13 horas.
Los demás isótopos poseen períodos de semidesintegración por debajo de las 10 horas y casi todos ellos sobreviven menos de un minuto. El Ac227 obtiene el equilibrio con sus productos de desintegración al finalizar los 185 días, luego se transmuta arreglándose a un periodo de semidesintegracion igual a 21,773 años.
¿Cómo se obtiene el Actinio?
Este elemento se obtiene en minerales de uranio en trazas de 227 Ac y con la reducción de fluoruro de actinio con vapor de magnesio, litio o calcio a 1100 – 1300 grados Celsius.
De igual forma se puede obtener con la desintegración de la uranitita (U308) y de 235 U, considerado como uno de los minerales más importantes de uranio. En estado sólido se produce con la reducción a altas temperaturas del fluoruro de actinio con vapores de litios.
Precauciones con el Actinio
El Ac227 es muy radiactivo, teniendo presentes sus efectos potenciales en la salud, su peligrosidad es similar a la del plutonio. Ingerir actinio, aún siendo en cantidades pequeñas, puede producir daños sumamente graves.

Vea también...