
Se caracteriza por ser un metal de transición de tonalidad gris, tiene gran dureza y una densidad baja. Posee gran resistencia a la corrosión por cloro, agua regia y agua del mar.
Este elemento es muy abundante en los depósitos de minerales, mayormente en apariencia de óxidos como la ilmenita y el rutilo, ambos distribuidos ampliamente en la litosfera y la corteza de la tierra. También es encontrado en los cuerpos de agua, seres vivos y objetos extraterrestres. La extracción de este elemento parte del mineral y se realiza a través del método de Hunter o metodo de Kroll.
El compuesto más popular es el dióxido de titanio, usado en la fabricación de pigmentos de tono blanco y en la fotocatálisis. Otros habituales compuestos son el componente catalizador de tetracloruro de titanio y el tricloruro de titanio que se usa para catalizar la producción de polipropileno.
Configuración Electrónica del Titanio
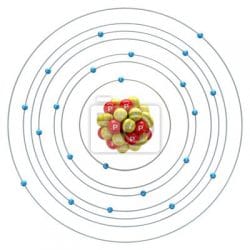
Con la configuración electrónica de cada elemento es posible especificar la manera en la que los electrones se encuentran estructurados en los átomos de dicho elemento.
En el caso del titanio, su radio medio es 140 pm, su radio covalente es 136 pm, su radio de Bohr o radio atómico es 176 pm. En total el titanio tiene 22 electrones, su distribución se hace de la siguiente forma: la primera capa posee 2 electrones, la segunda tiene 8, la tercera abarca 10 y en la cuarta hay 2 electrones.
Propiedades Físicas
El titanio es un elemento de metal tiene la proporción de densidad y dureza más grande. Este metal es fuerte, su densidad es baja y la ductilidad es alta, mayormente en ambientes donde no hay oxígeno. Su color es blanco metálico. Su punto de fusión está por encima de los 1650 grados Celsius, lo cual es relativamente alto permitiéndole ser de utilidad como metal refractario. Tiene baja conductividad térmica y eléctrica y es paramagnético.
Propiedades Químicas
Similar al magnesio y aluminio, el titanio junto a sus aleaciones tiende a oxidarse cuando se exponen al aire. El titanio tiene reacción con el oxígeno en temperatura de 1200 grados Celsius en el aire y en oxígeno puro a 610 grados Celsius, creando dióxido de titanio.
A pesar de esto, las reacciones de oxidación que se realizan en contacto con el agua y el aire son lentas por la pasivación que crea una capa de óxido que sirve de protección al metal en su oxidación propia. De forma inicial, cuando se crea esta capa de protección, sólo tiene entre 1 y 2 n, de grosor y aumenta lentamente de tamaño hasta llegar a los 25 nm en un lapso de cuatro años.
El titanio es sumamente resistente a la corrosión, se compara al platino porque puede resistir el ataque de fuertes ácidos minerales tales como el sulfúrico y demás oxoácidos de casi todas las soluciones de cloro y ácidos orgánicos. Pero los ataques concentrados de ácidos si crean una corrosión mayor. El titanio es muy reactivo termodinámicamente.
El metal empieza a arder antes de llegar al punto de fusión y esta misma únicamente puede darse en el vacío o en una atmósfera inerte. Tiene combinación con el cloro en una temperatura de 550 grados Celsius, teniendo reacción con los demás halógenos y absorbiendo hidrógeno.
Consiste en ser uno de los pocos elementos que pueden arder en nitrógeno puro teniendo reacción a una temperatura de 800 grados Celsius para crear nitruro de titanio, esto provoca pérdida de ductilidad en este material.

