Configuración electrónica del Lutecio
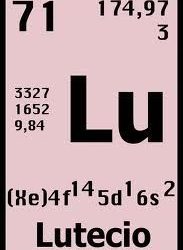
Aunque se encuentra en los elementos del bloque d, frecuentemente se incluye en los lantánidos, también llamados tierras raras porque tiene muchas propiedades con las que comparte similitudes. De todos estos, es el elemento más difícil para aislar. Por esta razón es escaso y tiene pocos usos en la actualidad.
El lutecio se caracteriza por ser un metal trivalente. Su tonalidad es plateada y blanca, resiste la corrosión y es relativamente estable cuando está en contacto con el aire. De todos los elementos de las tierras raras, ese es el más duro y pesado.
Este metal se usa como catalizador para el craqueo de petróleo de las refinerías y en distintos procesos químicos tales como la hidrogenación, la alquilación y la polimerización. Actualmente se investigan radioisótopos de lutecio para usarse en medicina nuclear de los tratamientos terapéuticos.
Configuración Electrónica del Lutecio

Con la configuración electrónica es posible saber la manera en la que se estructuran los electrones que pertenecen a los átomos del elemento. El lutecio se compone de 71 electrones y se distribuye así:
- La primera capa posee 2 electrones.
- La segunda capa alberga 8 electrones.
- La tercera capa está compuesta de 18 electrones.
- La cuarta capa tiene 32.
- En la quinta capa existen 9 electrones.
- En la sexta y última capa hay 2 electrones.
El radio de radio atómico del lutecio es de 217 pm, el radio medio es igual a 175 pm y el radio covalente corresponde a 160 pm. La masa atómica de cualquier elemento se define por la masa completa de protones y neutrones que se halla en un átomo de cualquier elemento. El lutecio posee una masa atómica igual a 174,967 u. La posición que tiene el lutecio en la tabla periódica es la del período 6 y el grupo 3.
Propiedades de la configuración del Lutecio
La forma natural del lutecio es el estado sólido. Este elemento químico tiene una tonalidad plateada y blanca, forma parte del grupo de los metales de transición. Su símbolo químico es Lu y su número atómico es 71.
El punto de ebullición de este elemento es de 3402,85 grados centígrados o grados Celsius, similar a 3675 grados Kelvin. El punto de fusión es igual a 1652,85 grados centígrados o grados Celsius, lo cual es igual a 1925 grados Kelvin.
Isótopos de Lutecio
El lutecio tiene un isótopo estable, este es Lu-175, su abundancia natural es de 97,41%. Existen 33 radioisótopos del lutecio identificados. Los de mayor estabilidad son el Lu-176, cuyo período de semidesintegración es igual a 3,78×1010 años y su abundancia natural es de 2,59%.
También está el Lu-174 con un período de semidesintegración igual a 3,31 años y por último el Lu-173 con 1,37 años. Los tiempos de semidesintegración de los demás isótopos radiactivos del lutecio son por debajo de 9 días, casi todos menores a media hora.
También hay 18 metaestados. Los de mayor estabilidad son Lu-178, Lu-174 y Lu-175. Sus periodos de semidesintegración respectivamente son 23,1 minutos, 142 días y 160,4 días.
Las masas atómicas que poseen los isótopos del lutecio tienen variaciones entre 149,973 uma perteneciente a Lu-150 y el Lu-184 de 183,962. La modalidad principal de desintegración que poseen los isótopos de mayor ligereza que el estable es a través de la captura electrónica, existiendo casos de desintegración α, a raíz de eso se producen isótopos de iterbio. Los isótopos de mayor peso que el estable son desintegrados a través de emisión β, esto resulta en isótopos de hafnio.
Obtención y Abundancia del Lutecio
La gran parte de las demás tierras raras son halladas en la naturaleza pero nunca de manera solitaria. El lutecio es el de menor abundancia en los elementos que se encuentran en la naturaleza. La mena principal de lutecio de forma comercialmente explotable se conoce como la monacita, la cual se compone de 0,003% de lutecio.
El metal puro no ha podido ser conseguido hasta finales del siglo pasado porque su preparación es demasiado complicada. El proceso llevado a cabo es intercambiar o reducir iones de LuF3 o de LuCl3 anhidro junto a metal alcalinotérreo o metal alcalino.
Precauciones con el Lutecio
Similar a las demás tierras raras, la toxicidad del lutecio es baja. Sin embargo este elemento y sus compuestos deben ser manipulados con máxima precaución. A pesar de que el lutecio no desempeña ninguna función biológica en el cuerpo humano, se tiene entendido que este crea estímulos en el metabolismo.

Vea también...