Ciclo del fosforo

En comparación con otros ciclos biogeoquímicos, como el ciclo del nitrógeno o el ciclo del carbono, este ciclo es sumamente lento al no dar lugar a la formación de compuestos volátiles que se desplacen con facilidad.
Ciclo del fosforo
Importancia del ciclo del fosforo
El fósforo es el segundo mineral más abundante del cuerpo humano, después del calcio.
- Es un nutriente esencial tanto para las plantas como para los animales. Su limitación restringe el crecimiento de los ecosistemas acuáticos.
- Aunque el fósforo se encuentre poco presente en el cuerpo de los seres vivos, juega un papel importante, ya que, forma parte de las macromoléculas de mayor importancia:
- ADN (ácidos nucleico).
- ARN (Ácido ribonucleico).
- ATP (Adenosin trifosfato).
- Además de encontrarlo en los dientes, los huesos y las células tienen un rol fundamental en el proceso de fotosíntesis.
- El fósforo proporciona estructura a las membranas celulares, tiene participación en la homeostasis, transporta energía a las células, transmite señales y, además, regula la actividad enzimática.
- Como consecuencia, el fósforo resulta imprescindible a nivel bioquímico para la obtención de energía y la transmisión hereditaria.
- En resumen, el ciclo del fósforo es un proceso importante que involucra la hidrosfera, la litosfera y la biosfera para el pase del fósforo hacia los distintos ecosistemas; Es muy apreciado como abono en la agricultura.
Características del ciclo del fósforo
- El fósforo es un elemento químico, no metálico, con símbolo P y número atómico 15.
- Se encuentra en los ácidos nucleico.
- Se encuentra en los animales, más específicamente en sus huesos, tejidos y dientes.
- No forma compuestos volátiles.
- Se usa esencialmente en la agricultura.
- Se convierte en portador de luz.
- Puede ser combinado con muchas sustancias.
- Es un elemento sedentario, en el cual su principal depósito son las rocas.
- Se oxida con el oxígeno.
¿Cuáles son las reservas del fósforo?
La principal reserva del fósforo la encontramos la en la corteza terrestre, principalmente en las rocas, a partir de las cuales, este elemento pasa a otras partes de los ecosistemas y a los seres vivos que en él se encuentran.
En la hidrosfera, el guano y sedimentos formados por excremento, específicamente, de aves marinas, minerales del grupo de los fosfatos y compuestos oceánicos formados por restos de seres vivos.
Etapas del ciclo del fosforo
Erosión y meteorización
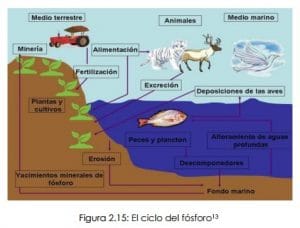
Ya que el fósforo abunda en los minerales terrestres y los encontrados en el fondo de los mares, los efectos de la erosión solar y eólica, así como, los efectos constantes de la lluvia permiten que las reservas fosfóricas salgan a la superficie y en consecuencia sean transformados a los diferentes ecosistemas.
Fijación en las plantas y transmisión en los animales
El fósforo encontrado en los suelos es absorbido por las plantas terrestres, las algas y el fitoplancton (aguas marinas), estas a su vez lo fijan a su organismo. El fósforo es transmitido a los animales que se alimentan de estas plantas y más tarde, los animales que se alimentan de los animales que ingirieron el fósforo encontrado en las plantas pasan a contener fósforo en su organismo y así se pasa de cadena en cadena.
Descomposición y retorno al suelo
Las aves que se alimentan de peces producen guano (excremento). El excremento se utiliza como fertilizante y es rico en fósforo; las excreciones de los animales son ricas en compuestos orgánicos, que pasan a ser útiles y aprovechables por las plantas y transmisibles al suelo al ser descompuestos por bacterias.
Cuando los animales mueren se descomponen en la tierra y los fosfatos retornan al suelo, las plantas lo absorben o los fosfatos se mueven hacia el mar o los ríos por la lluvia.
Sedimentación y retorno al suelo
La sedimentación, es otra vía de retorno del fósforo a la tierra que consiste en la fosilización de los restos orgánicos, volviendo a formar parte de los minerales sedentarios.
Contenido del artículo

Vea también...